التيقظ الدوائي (Pharmacovigilance) هو خط الدفاع الأخير الذي يحمي الأفراد من الآثار غير المتوقعة للأدوية. هذا العلم ليس مجرد إجراء إداري، بل هو نظام عالمي دقيق، وُلِد من رحم سلسلة من الكوارث الدوائية التي غيرت مسار التشريع الصحي، ليترسخ اليوم كركيزة أساسية في الأنظمة الصحية المتقدمة، وعلى رأسها منظومة المملكة العربية السعودية بقيادة الهيئة العامة للغذاء.
وفقًا لمنظمة الصحة العالمية، فإن التيقظ الدوائي (Pharmacovigilance) هو:
“العلم والأنشطة المتعلقة باكتشاف وتقييم وفهم ومنع الآثار الجانبية الضارة للأدوية وأي مشكلة أخرى محتملة تتعلق بها”.

يؤكد هذا التعريف أن التيقظ الدوائي ليس مجرد مجموعة إجراءات (أنشطة)، بل هو مجال علمي قائم بذاته يتطلب تخصصاً وبحثاً. التيقظ الدوائي له أربع مراحل جوهرية (اكتشاف، تقييم، فهم، منع):
• الاكتشاف (Detection): يشير إلى عملية الرصد وجمع البلاغات عن الأعراض الجانبية غير المتوقعة أو المعروفة.
• التقييم (Assessment): يعني تحليل البيانات المجمعة لتحديد العلاقة السببية بين الدواء والحدث الضار.
• الفهم (Understanding): يركز على الجانب العلمي والبحثي، مثل فهم الميكانيكية التي تسبب بها الدواء هذا الضرر، وهو أمر حيوي لتعزيز المعرفة الطبية.
• المنع (Prevention): وهو الهدف النهائي والأكثر أهمية، ويعكس الجانب الاستباقي للتيقظ الدوائي، حيث يتم اتخاذ إجراءات تنظيمية (تعديل النشرة، سحب الدواء، تثقيف) لمنع تكرار الضرر.
الميلاد من رحم الكارثة.. صدمات صنعت اليقظة العالمية
لم يكن التيقظ الدوائي نظاماً إلزامياً قبل منتصف القرن العشرين. كانت الثقة المطلقة في التجارب السريرية السابقة للتسويق هي السائدة، وهي ثقة ثبت أنها في غير محلها تماماً.
إلكسير السلفانيلاميد: أول إنذار حول المركبات غير الفعالة
في عام 1937، عاشت الولايات المتحدة أول مأساة دوائية كبرى، قدمت الدرس الأول عن خطورة الإهمال في اختبار مكونات الدواء غير الفعالة (Excipients). القصة تتعلق بدواء السلفانيلاميد، وهو مضاد حيوي فعال، حيث قررت شركة “S.E. Massengill Co” تصنيع نسخة سائلة منه للأطفال. استخدم المصنعون مادة ثنائي إيثيلين جلايكول (Diethylene Glycol – DEG) كمذيب لمذاقها الحلو، وهي مادة سامة جداً ولم تخضع لاختبارات السلامة.
استخدام هذا المذيب القاتل أدى إلى كارثة صحية سريعة، حيث توفي أكثر من 100 شخص، معظمهم من الأطفال الأبرياء، نتيجة الفشل الكلوي الحاد الناتج عن التسمم بـ (DEG).
العبرة التشريعية: أدت هذه المأساة مباشرةً إلى إصدار قانون الغذاء والدواء ومستحضرات التجميل الفيدرالي لعام 1938 (FD&C Act)، والذي ألزم مصنعي الأدوية ولأول مرة بتقديم دليل علمي على مأمونية الدواء قبل السماح بتسويقه.

كارثة الثاليدوميد: التوقيت الحاسم والميلاد العالمي (1957 – 1961)
القصة المحورية التي أرست قواعد التيقظ الدوائي عالمياً هي قصة الثاليدوميد. هذا الدواء الذي سُوِّق كمهدئ وعلاج لغثيان الحمل، أدى خلال أربع سنوات فقط إلى ولادة ما يقدر بـ 10,000 طفل مشوه حول العالم بتشوهات خلقية مروعة، أبرزها عدم اكتمال الأطراف (الفقمة).
القصة الملهمة: كانت الدكتورة فرانسيس أولدهام كيلسي، في هيئة الغذاء والدواء الأمريكية، البطلة التي رفضت ترخيص الدواء في عام 1960 لعدم اقتناعها ببيانات مأمونية الاستخدام على الحوامل، منقذة آلاف الأجنة الأمريكية. دفعت هذه الكارثة منظمة الصحة العالمية إلى تأسيس مركز أوبسالا لمراقبة الأدوية (UMC) في السويد عام 1968، لتبدأ مرحلة الرصد العالمي المنظم.
سحب الفيوكس: العبرة في المراقبة طويلة الأجل
في العصر الحديث، جاء سحب دواء فيوكس (Vioxx) في عام 2004 ليؤكد أن المأمونية ليست مرحلية بل عملية مستمرة. فبعد سنوات من الاستخدام، كشفت الدراسات الوبائية طويلة الأمد عن أن هذا المسكن يزيد من مخاطر النوبات القلبية والسكتات الدماغية. هذا السحب رسخ مفهوماً جديداً وهو خطط إدارة المخاطر (RMPs)، التي أصبحت إلزامية لشركات الأدوية.

التيقظ الدوائي في المملكة العربية السعودية
1. الإلزام بالشخص المؤهل للتيقظ الدوائي (QPPV):
في نوفمبر 2010، ألزمت الهيئة جميع الشركات التي تحصل على ترخيص تسويق لمستحضر صيدلي في المملكة بتعيين “الشخص المؤهل للتيقظ الدوائي” (Qualified Person for Pharmacovigilance – QPPV). هذا المتخصص هو المسؤول الأول عن نظام التيقظ الدوائي للشركة أمام الهيئة. وتم تعزيز هذا التوجه بقرار سعودة وظيفة الـ (QPPV) في أكتوبر 2014.
2. خطط إدارة المخاطر (RMPs) ودراسات السلامة (PASS):
تُعد خطط إدارة المخاطر (RMPs) وثيقة إلزامية تراجعها الهيئة، تحدد كيفية إدارة مخاطر الدواء على مدار دورة حياته. ويشمل ذلك تحديد إجراءات المراقبة الفعالة، والتي قد تتطلب إجراء دراسات السلامة بعد الترخيص (PASS). هذه الدراسات هي دراسات وبائية أو قائمة على الملاحظة، تُلزم بها الهيئة الشركة بعد طرح الدواء في السوق للإجابة على أسئلة محددة حول مأمونية الدواء لم يتمكن الباحثون من الإجابة عنها خلال التجارب السريرية، مثل قياس معدل حدوث تأثير جانبي نادر أو تقييم مأمونية الدواء في فئات معينة من المرضى.

منصة “تيقظ”: قلب التيقظ الدوائي الرقمي في المملكة
في عام 2014، شكل إطلاق المركز الوطني للتيقظ والسلامة الدوائية وإطلاق منصته الرقمية “تيقظ” نقلة نوعية في منهجية الرصد الدوائي بالمملكة. “تيقظ” هي منظومة رقمية متكاملة متاحة للممارس الصحي والمستهلك العادي على حد سواء، عبر تطبيق إلكتروني وموقع على الإنترنت.
المنصة لا تقتصر على الآثار الجانبية للأدوية البشرية فحسب، بل توسع نطاق رصدها ليغطي أربعة محاور أساسية: الأدوية البشرية، والأخطاء الدوائية، ومشاكل جودة وفعالية المستحضرات الدوائية، والمنتجات الصحية الأخرى كالأجهزة الطبية ومستحضرات التجميل. هذه الشمولية تضمن أن تكون رؤية الهيئة لمأمونية السوق شاملة وسريعة.
يُعد اكتشاف الإشارة (Signal Detection) قلب عملية التيقظ الدوائي وأكثر مراحلها أهمية وتعقيداً. الإشارة، ببساطة، هي معلومات مبلغ عنها عن وجود علاقة سببية محتملة بين حدث ضار معين ودواء ما، بحيث تكون هذه العلاقة غير معروفة مسبقاً أو غير موثقة بشكل كامل.
هدف هذه العملية ليس مجرد جمع البيانات، بل تحليل الكم الهائل من البلاغات التلقائية (Spontaneous Reports) الواردة من الأطباء والصيادلة والجمهور (عبر منصات مثل “تيقظ”)، ومن قواعد البيانات العالمية (مثل VigiBase)، لتحديد أي نمط غير عادي أو زيادة غير متوقعة في تكرار حدوث عرض جانبي معين.
يعتمد هذا الاكتشاف على تقنيات إحصائية متقدمة، تُعرف باسم تحليل عدم التناسب (Disproportionality Analysis). إذا كان الارتباط مرتفعاً بشكل غير متناسب، يتم إطلاق “إشارة” تتطلب تحقيقاً وبائياً عميقاً لـ تقييمها وتأكيدها قبل اتخاذ أي قرار تنظيمي نهائي، وهي تمثل الدرع الواقي ضد المخاطر الدوائية المستجدة.
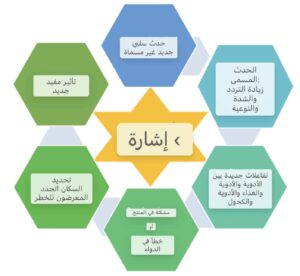
ما هي الإشارة؟
يمكن أن تكون الإشارة زيادة في التردد / الشدة / الخصوصية لحدث موسوم أو حدث سلبي جديد غير مصنف أو تفاعلات محددة حديثا بين الأدوية / المخدرات – الكحول أو خطأ الدواء / مشكلة المنتج أو تحديد مجموعة سكانية جديدة معرضة للخطر أو تأثير مفيد جديد للدواء.
المعلومات التي تنشأ من مصدر واحد أو عدة مصادر (بما في ذلك الملاحظات والتجارب)، والتي تشير إلى وجود علاقة سببية جديدة محتملة، أو جانب جديد من الارتباط المعروف، بين التدخل وحدث أو مجموعة من الأحداث ذات الصلة، سواء كانت سلبية أو مفيدة، والتي تعتبر ذات احتمال كاف لتبرير إجراء التحقق.
آليات العمل والمشاركة المجتمعية
يعتمد التيقظ الدوائي في السعودية على شبكة واسعة من الجهات. تُشكل هيئة الغذاء والدواء (SFDA) النواة، مع مركزها الوطني للتيقظ الدوائي الذي يدير عمليات التحليل والتقييم. يشمل الإبلاغ الإلزامي للأطباء، الصيادلة، والممرضين عن أي اعراض جانبية للدواء (ADRs)، بالإضافة إلى تشجيع المرضى على الإبلاغ عبر تطبيق “تواصل” التابع لـ (SFDA). في 2023، أدخلت الهيئة حملة “أبلغ عن الآثار الجانبية”، التي بلغت تغطيتها 80% من المنشآت الصحية، مما أدى إلى زيادة الإبلاغات من قبل المواطنين بنسبة 40%.
من الناحية التقنية، يستخدم النظام الذكاء الاصطناعي لتحليل البيانات الكبيرة، مما يساعد في كشف الأنماط المبكرة للمخاطر. على سبيل المثال، خلال حملة التطعيم ضد كوفيد-19، رصدت (SFDA) أكثر من 50,000 تقرير عن آثار جانبية للقاحات، مما سمح بتعديل الإرشادات الطبية بسرعة، وأكدت الفعالية العالية للقاحات المستخدمة. كما تعاونت (SFDA) مع شركات الأدوية مثل (Pfizer) و(AstraZeneca) لمراقبة المنتجات الجديدة، حيث يُطلب من الشركات تقديم تقارير دورية عن السلامة.
تشمل المشاركة المجتمعية برامج تدريبية واسعة. أطلقت (SFDA) أكاديمية التيقظ الدوائي في 2020، التي دربت أكثر من 10,000 متخصص صحي حتى 2025. كما أقامت شراكات مع جامعات مثل جامعة الملك سعود وجامعة الإمام، لدمج مقررات التيقظ الدوائي في البرامج الطبية والصيدلانية. هذه الجهود ساهمت في رفع الوعي، حيث أظهر استطلاع (SFDA) في 2024 أن 65% من الأطباء يبلغون عن (ADRs) بانتظام، مقارنة بـ 30% في 2015.
على المستوى الدولي، ساهمت السعودية في برنامج (WHO) للقاحات، حيث قدمت بياناتها عن (ADRs) للقاحات كوفيد-19 إلى قاعدة (VigiBase)، مما ساعد في تحديث الإرشادات العالمية.
اقتصاديًا، يُقدر أن التيقظ الدوائي وفر على النظام الصحي السعودي أكثر من 500 مليون ريال سنويًا من خلال تجنب التكاليف الناتجة عن المضاعفات الدوائية، وفقًا لدراسة نشرتها (SFDA) في 2024.
من الإنجازات البارزة أيضًا، إطلاق “دليل السلامة الدوائية” الإلكتروني في 2023، الذي يوفر معلومات فورية عن 5,000 دواء، متاحًا للأطباء والمرضى. هذا الدليل ساهم في تقليل الأخطاء الدوائية بنسبة 25% في المستشفيات الحكومية، كما أفاد تقرير وزارة الصحة.
آفاق المستقبل.. اليقظة الذكية والتحديات المستمرة
يتجه مستقبل التيقظ الدوائي في المملكة نحو استخدام التكنولوجيا المتقدمة لمواجهة التحديات المزمنة:
• التحول الرقمي والذكاء الاصطناعي: تسعى الهيئة لتوظيف أدوات الذكاء الاصطناعي (AI) في معالجة وتحليل بلاغات التيقظ الضخمة. هذا التطور يهدف إلى تسريع عملية “اكتشاف الإشارة” بشكل استباقي وفعال، وتقليل الوقت اللازم لاتخاذ القرار التنظيمي.
• اليقظة الشاملة: تعمل الهيئة على توسيع نطاق اليقظة ليشمل الأجهزة الطبية والمستحضرات التجميلية بشكل أكثر تكاملاً، لضمان أعلى مستويات الأمان.
التحدي الأكبر: يبقى التحدي الأبرز هو النقص في الإبلاغ (Under-reporting) من قبل بعض الممارسين الصحيين. لذا، تواصل الهيئة جهودها التدريبية والإلزامية لضمان أن كل حالة عرض جانبي يتم توثيقها والإبلاغ عنها، لأن كل بلاغ هو حجر زاوية في بناء المأمونية الدوائية الوطنية.
في الختام، يُعد التيقظ الدوائي في السعودية قصة نجاح مستمرة، تحولت من جهود محدودة إلى نظام متكامل يحمي آلاف الأرواح. مع إنجازاته في مواجهة الجائحات والأدوية الجديدة، وزيادة الإبلاغات إلى أكثر من 200,000 تقرير متوقع في 2025، ومواجهة تحدياته بحكمة، يُمثل هذا المجال نموذجًا للدول النامية.
في النهاية، يظل التزام (SFDA) والمجتمع الصحي بمراقبة السلامة الدوائية هو الضمان الأمثل للصحة العامة. إن استمرار الاستثمار في هذا المجال ليس خيارًا، بل ضرورة لمستقبل صحي مستدام.

 علوم القطيف مقالات علمية في شتى المجالات العلمية
علوم القطيف مقالات علمية في شتى المجالات العلمية
